急性心肌梗死严重威胁威胁人类健康,由于成人心脏再生能力有限,心梗出现的大量心肌细胞死亡会被纤维瘢痕替代,进一步引发心律失常和心力衰竭。如何改善缺血损伤区心肌细胞的存活、再生和心肌重构一直是研究人员关注的重点。
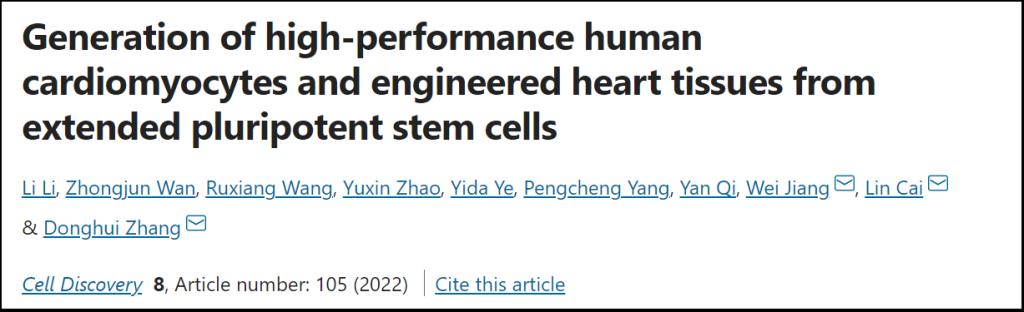
湖北大学科研团队与武汉大学科研团队经过努力研究,证实扩展多能干细胞(ESPC)是一种新的高效获取人源心肌细胞的种子细胞,提供了相应衍生心肌细胞的制备方法,并验证其对于心肌缺血损伤修复的促进作用,有助于干细胞在心脏疾病发生、药物筛选以及心脏再生医学方面的应用研究。近日,该研究成果以“Generation of high-performance human cardiomyocytes and engineered heart tissues from extended pluripotent stem cells”(扩展干细胞来源的高质量人源心肌和工程化心肌组织)为题,登上国际学术期刊Cell Discovery(影响因子 IF=38.08)。湖北大学生命科学学院张冬卉教授、蔡琳讲师和武汉大学蒋卫教授为本文通讯作者,湖大博士生李俐和硕士生万忠均为该论文共同第一作者,湖大研究生汪如香、赵宇鑫、叶一达、杨鹏程、齐炎等作出了重要贡献。
首次将人扩展性多能干细胞(EPSC)诱导为心肌细胞
该研究报道了将多个EPSC系首次成功分化为心肌细胞的方法,并证明由EPSC衍生的心肌细胞(EPSC-CM)与ESC/iPSC衍生心肌相比,具有更成熟的肌节结构和线粒体形态功能;同时利用水凝胶工程化心肌组织构建体系证实EPSC-CM衍生的心肌微组织钙传导能力和力学收缩性能表现更优。更重要的是,EPSC-CM移植至心梗的裸大鼠心肌6周后可以显著改善心脏功能并降低梗死面积。该研究进一步证明了EPSC在心脏研究领域的应用潜力,为EPSC来源的心肌细胞可能成为缺血性心肌病的治疗提供理论基础和依据。
去年7月,蒋卫教授与张冬卉教授以及华中农业大学苗义良教授合作,在Stem Cell Reports杂志发表了将常规hiPSC转化为无需饲养层细胞的EPSC的方法,并从表观和代谢角度优化建立了一种新的培养方案,可以在体外稳定培养EPSC细胞100代以上(Stem Cell Reports 16, 1686-1696)。
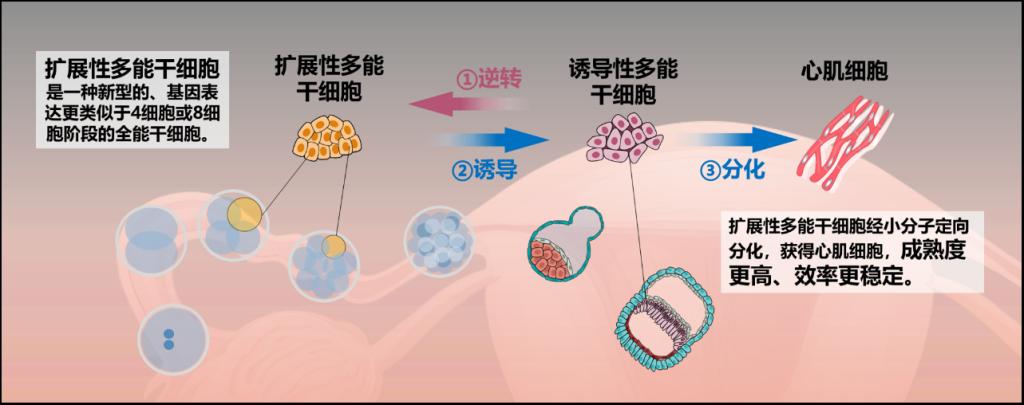
本研究在此基础上,对人胚胎干细胞系H9和诱导多能干细胞系WTC来源的EPSC尝试心肌分化,探索多种途径后发现通过对EPSC用mTeSR1或RPMI 1640 + B27 + FGF2 + TGFβ体系预分化2-3天后再定向诱导心肌分化可以高效获得CTNT阳性的心肌细胞。值得一提的是,对比不同干细胞连续10批次的分化效率,EPSCs的分化条件容忍度和多批次稳定性均明显高于iPSC/ESC。
用于心肌缺血损伤治疗
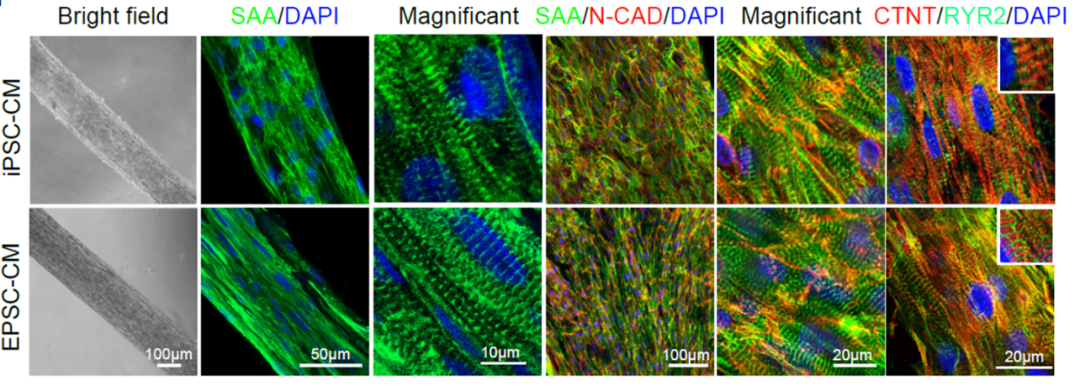
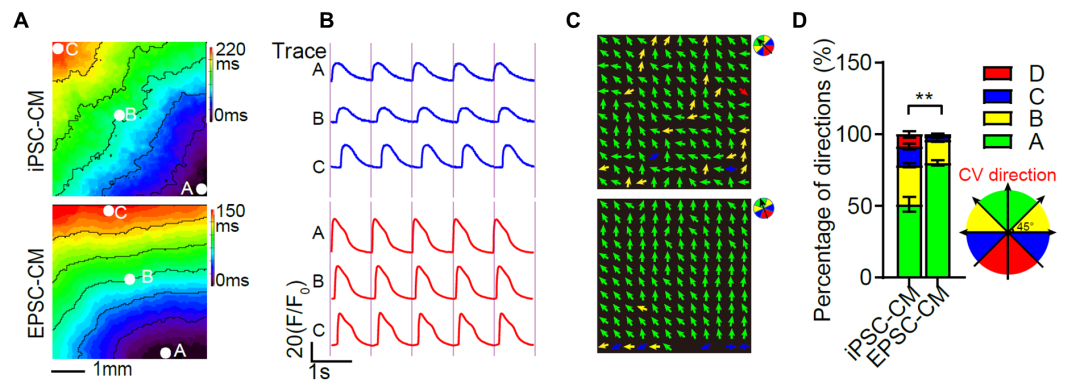
团队进一步详细对比了EPSC衍生心肌与iPSC/ESC衍生心肌细胞在平面和三维微组织层面上的细胞形态、线粒体功能、钙传导和收缩力等功能特征,在同等培养时间和条件下, EPSC-CM表现出更好的均一性和功能成熟度 。进一步进行体内功能验证,在裸大鼠心梗造模后移植两种心肌细胞并观察六周,结果显示EPSC-CM可明显改善心功能和降低心肌梗死面积,同时细胞移植区域的心肌纤维化程度和心肌细胞凋亡比率均低于iPSC-CM组, 提示移植EPSC-CM更有利于改善心肌缺血损伤 。
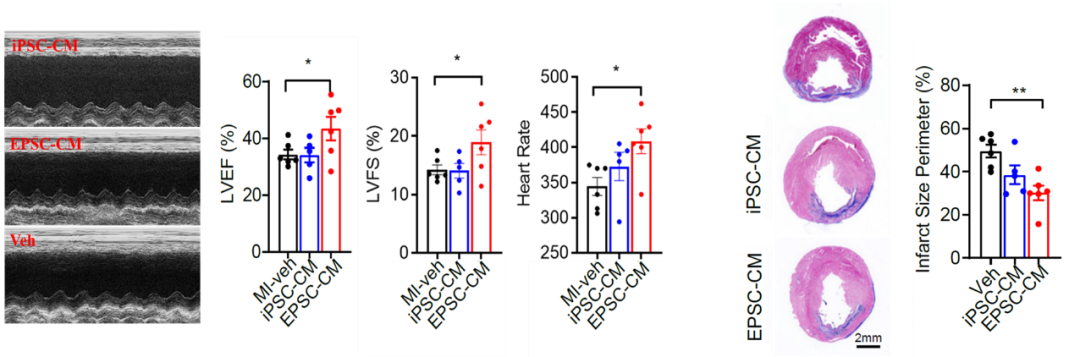
本研究证实EPSC是一种新的高效获取人源心肌细胞的种子细胞,提供了EPSC-CM的制备方法,并验证其对于心肌缺血损伤修复的促进作用,有助于干细胞在心脏疾病发生、药物筛选以及心脏再生医学方面的应用研究。
EPSC研究背景
如何改善缺血损伤区心肌细胞的存活、再生和心肌重构一直是研究人员关注的重点。人诱导多能干细胞(iPSC)是一类备受关注的种子细胞,在疾病模型构建、药物筛选和细胞治疗方面有广阔应用前景。自2011年通过化学小分子调控WNT信号体外诱导iPSC分化为心肌细胞方法成功建立后,利用iPSC来源的心肌细胞研究心脏疾病和心脏功能修复取得快速进展,但目前仍存在iPSC细胞异质性高、分化效率不稳定、心肌细胞成熟度低等问题。
扩展多能干细胞(EPSC)在2017年由北京大学邓宏魁教授团队和剑桥大学刘澎涛教授团队分别建立并证明是具有比iPSC更佳发育潜能的干细胞(Cell 169, 243-257; Nature 550, 393-397),其单细胞克隆率高、高效的嵌合能力和胚外组织发育能力受到广泛关注。2020年邓宏魁教授团队报道EPSC体外诱导分化的肝细胞具有成熟的分泌功能,且基因转录组比iPSC来源的肝细胞更类似于人的原代肝细胞。但EPSC能否定向分化为中胚层的心肌细胞,以及EPSC来源的心肌细胞是否会有更优异的功能均尚未可知。

张冬卉教授课题组基于人多能干细胞定向诱导分化、基因编辑、组织工程、微组织生理功能检测等底层技术,开发以心肌微器官为主,包括瓣膜类器官在内的生理、病理研究模型,并基于此,研究遗传性心肌病、心肌梗死、心律失常、心衰、瓣膜钙化、组织纤维化的致病机理,挖掘病程的干预靶点、开发出新型诊疗方案。先后在Cell Research、Nature Review Cardiology、Circulation、Circulation Research、Redox Biology等国际主流杂志发表数十篇文章,SCI总引用次数超过2000次。
(审稿:谢玉平)